Натрий Na
Натрий в таблице менделеева занимает 11 место, в 3 периоде.| Символ | Na |
| Номер | 11 |
| Атомный вес | 22.9897693 |
| Латинское название | Natrium |
| Русское название | Натрий |
Электронная схема натрия
Na: 1s2 2s2 2p6 3s1
Короткая запись:
Na: [Ne]3s1
Одинаковую электронную конфигурацию имеют атом натрия и Si+3, P+4, S+5, Cl+6
Порядок заполнения электронами оболочек атома натрия (Na): 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘p’ - до 6, на ‘d’ - до 10 и на ‘f’ до 14
Натрий имеет 11 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
1 электрон на 3s-подуровне
Степень окисления натрия
Атомы натрия в соединениях имеют степени окисления 1, -1.
Степень окисления - это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Ионы натрия
Валентность Na
Атомы натрия в соединениях проявляют валентность I.
Валентность натрия характеризует способность атома Na к образованию химических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Na
Квантовые числа определяются последним электроном в конфигурации, для атом Na эти числа имеют значение N = 3, L = 0, Ml = 0, Ms = +½
Видео заполнения электронной конфигурации (gif):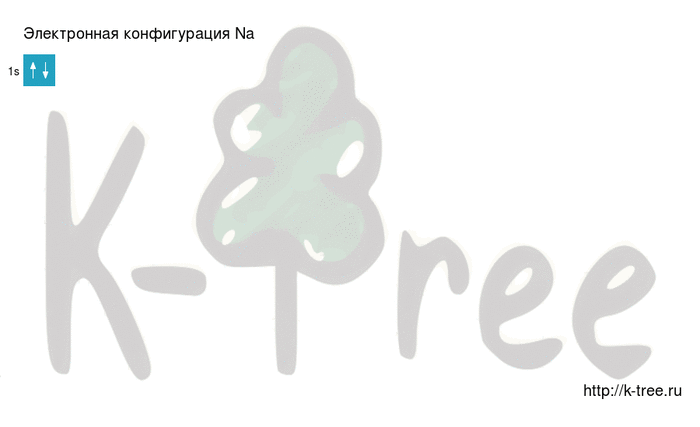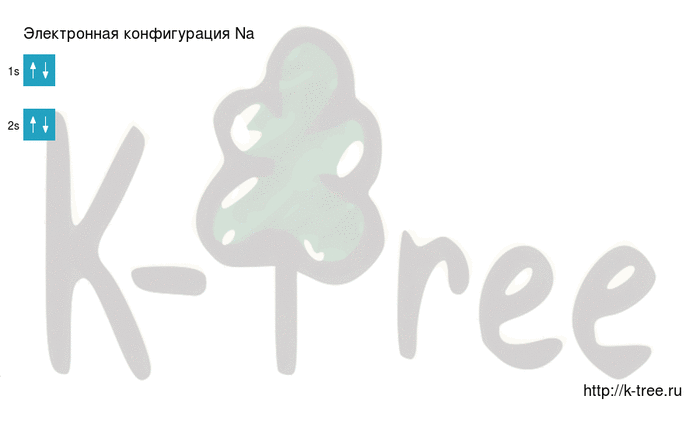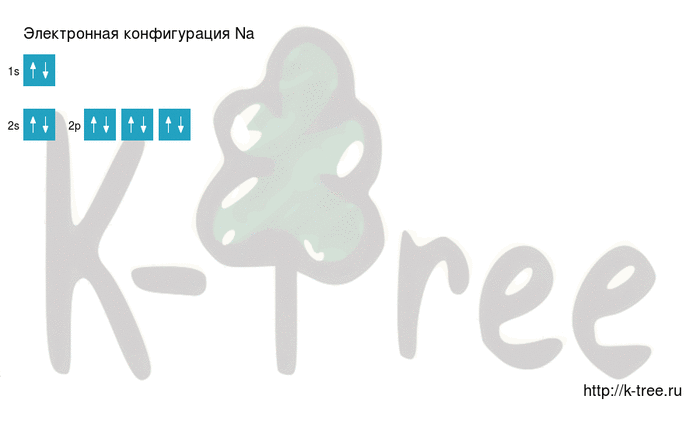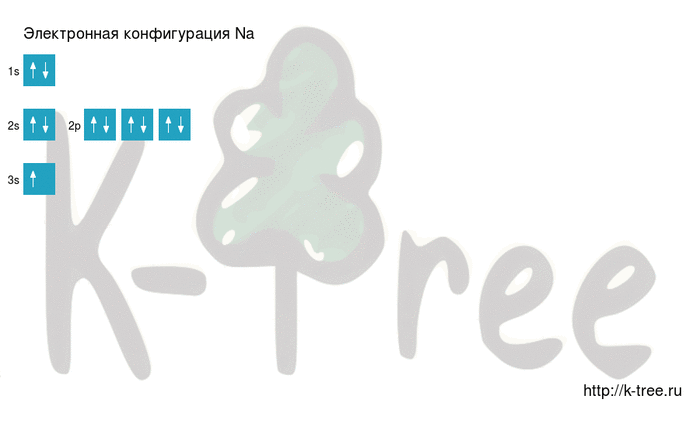
Результат:

Соединения натрия
| Тип | Формула | Название |
|---|---|---|
| Соль | NaHCO3 | Пищевая сода |
| Основание | NaOH | Гидроксид натрия |
| Минерал | FeCr2O4 | Хромит |
Энергия ионизации
Чем ближе электрон к центру атома - тем больше энергии необходимо, что бы его оторвать. Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo. Если не указано иное, то энергия ионизации - это энергия отрыва первого электрона, также существуют энергии ионизации для каждого последующего электрона.
Энергия ионизации Na:
Eo = 495 кДж/моль
Перейти к другим элементам таблицы менделеева
Где Na в таблице менделеева?Таблица Менделеева
Скачать таблицу менделеева в хорошем качестве
